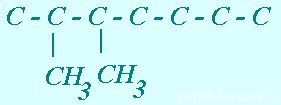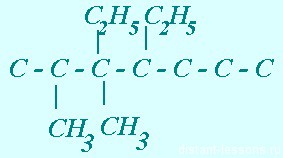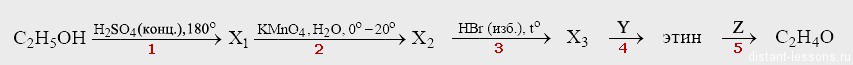Номенклатура ИЮПАК (IUPAK)
IUPAC — International Union of Pure and Applied Chemistry
Номенклатура ИЮПАК (IUPAC)— это правила названий соединений, общие во всем мире.
С номенклатурой неразветвленных органических соединений все понятно — первая часть названия соответствует количеству атомов, вторая — классу соединения, например, бутан — 4 атома углерода, алкан.
У разветвленных соединений номенклатура посложнее. Есть определенные общие правила.
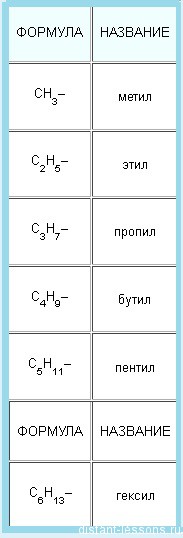
«Ответвления» от основной цепи называются радикалы. В таблице приведены названия основных радикалов. По сути это частицы без одного атома H. Их названия соответствуют названиям алканов, только с другим окончанием — -ил.
1. Главная углеродная цепь, во-первых, должна быть самой длинной, во-вторых, если имеются две или более одинаковые по длине цепи, то из них выбирается наиболее разветвленная.
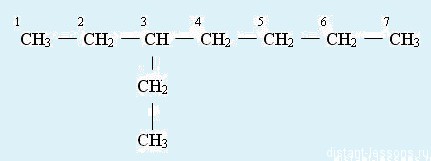
2. Нумерацию начинают с того атома углерода, к которому ближе радикал.
3. Указывают номер атома, при котором крепится радикал, называют радикал, называют саму цепь: 3-этилгептан.
Если радикалов несколько, то их называют в алфавитном порядке, указывая «место крепления» каждого:
Если в соединении несколько одинаковых радикалов, то добавляют приставки-числа: ди-, три-, тетра- и т.д.
Иногда встречаются задания, в которых по названию нужно написать структурную формулу вещества. Здесь нужно использовать номенклатуру ИЮПАК «с конца».
Дано вещество: 2,3-диметил, 3,4диэтил гептан
Начинаем «с конца» -сначала рисуем цепь из 7 атомов углерода с одинарными связями- гептан:
С — С — С — С — С — С — С
Нам дано, что при втором и третьем атоме у него радикалы — 2 метила:
Так же пририсовываем 2 этила — у 3-го и 4-го атомов С (я их нарисовала вверху молекулы, чтобы места хватило):
Осталось только доставить атомы водорода. Принцип простой — у каждого углерода должно быть 4 связи (часто радикалы пишут в скобках рядом с теми атомами, при которых они находятся)):
СH3-С(CH3)-C(CH3)(C2H5)-C(C2H5)-CH2-CH2-CH3
Обратите внимание: есть атомы углерода «концевые» — они окружены тремя водородами (-CH3). У них только 1 связь с другим атомом углерода. Такие атомы по классификации ИЮПАК называются первичными.
Если у атома углерода 2 связи с другими С — это вторичный атом углерода (-CH2-).
Три — третичный (-C) и т.д.
Для чего была разработана номенклатура ИЮПАК? Часто математику называют универсальным языком мира. Числа и математические формула понятны в любой стране, для любого иностранца. Так вот, номенклатура ИЮПАК — это такой своеобразный международный язык, только понимают его химики :).
Основы органической химии
Основы органической химии
Традиционно органическими веществами называют соединения углерода.
Но CO2 и CO- это тоже соединения углерода
Органические соединения — это соединения, в которых есть углеродные цепи, т.е. есть связь С-С и связи с другими элементами (у алмаза, например, тоже есть связи С-С, но нет других элементов).
«Другие элементы» — это, в основном, H, O, N, S и др.
Многие думают, что органическая химия — это химия «природных веществ» — таких как белки, жиры, углеводы и т.д. Но полиэтилен — то, из чего делают обычные пакеты, в которые мы продукты упаковываем, это тоже органическое вещество.
У всех органических веществ есть общие свойства:
1. Связь -С-С- и связи углерода с указанными выше элементами.
2. В органической химии есть понятие изомерия.
Изомеры — одинаковые по составу и молекулярной массе вещества, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам.
В принципе, очень похоже на аллотропию — у алмаза, графита и карбина, например, тоже одинаковый качественный и количественный состав, и свойства у них совсем разные, но аллотропия — свойство присущее только простым веществам, а органические вещества (см. пункт 1) — сложные.
3. Все-все все органические вещества сгорают до CO2 и H2O
4. Реакции в органической химии протекают медленно, не всегда до конца, большинство органических соединений малоактивны.
5. У органических соединений низкие температуры плавления, кипения, разложения.
В основном, реакции в органической химии идут по функциональным группам, по этим группам вся органическая химия делится на классы веществ:
- Углеводороды (по названию, содержат только С и Н):
алканы (имеют одинарную связь между атомами С),
циклоалканы (циклические соединения с одинарными связями между атомами углерода),
алкены (содержат двойную связь >С=С<),
алкины ( -C ≡ C-)
алкадиены (-С=С-С=С-)
и
ароматические углеводороды (ароматическая связь, шестичленное кольцо из атомов углерода).
- Кислородсодержащая органика:
Спирты и фенолы (функциональная группа -OH);
Альдегиды (функциональная группа -COH — собственно альдегиды и -С=О -кетоны);
Карбоновые кислоты (-COOH)
- Азотсодержащие органические вещества:
Нитросоединения (содержат группу -NO2)
Производные аминов (-NH2)
Это те соединения, которые рассматривают в школьном курсе химии — в 10 и 11 классах. Конечно, классов намного больше и некоторые из них рассмотрим и с биологической стороны, т.к. их роль в обмене веществ огромна.
Итак, начинаем изучать органическую химию!
Как эффективно подготовиться к экзамену
Вопрос «Как эффективно подготовиться к экзамену» мне задают ОЧЕНЬ часто, есть несколько мнений по этому поводу, я озвучу здесь свое личное мнение, которое за 7 лет работы принесло определенные хорошие результаты.
Задачи на фенолы
Задачи на фенолы
Фенолы отличаются от алифатических спиртов наличием бензольного кольца и исключительно кислотными свойствами -OH — группы (т.е. отщепляется только водород).
Задачи на фенолы пример №1
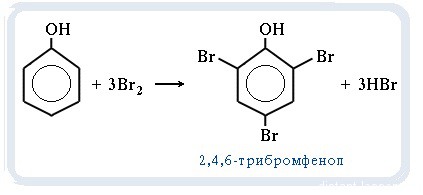
Внимание: с бромной водой будет реагировать только фенол (качественная реакция) !
С6H5-OH + Br2 = C6H4Br(OH) + HBr
Т.е. выпавший осадок массой 33.1 г — 2,4,6-бромфенол.
n(C6H2Br3(OH))=m\Mr=33.1\331 = 0.1 моль
n(C6H5OH)=n(C6H2Br3(OH))= 0.1 моль
m(C6H5OH)=n*Mr = 0.1*94=9.4 г
Значит, масса ароматического углеводорода m = m(cмеси) — m(C6H5OH) = 14-9.4 = 4,6 г
Mr(CnH2n-6)= m\n=4,6 \ 0.05 = 92
Подставляем значение молярной массы в общую формулу аренов:
12n + 2n -6 = 92
14n=98
n=7
C7H8 — толуол
Задачи на фенолы пример №2
|
При обработке 4,18 г смеси бензилового спирта, крезола и фенола избытком калия выделилось 448 мл (н.у.) газа. Вычислите массовую долю фенола в исходной смеси.
|
Итак, сначала определимся с формулами:
бензиловый спирт: С6H5CH2OH:
крезол: С6H4(CH3)OH
фенол: С6H5OH:
Бензиловый спирт С6Н5СН2ОН и крезол СН3С6Н4ОН являются изомерами состава С7Н8О. Их массу в смеси обозначим через х, а объем выделившегося водорода – у, тогда реакцию изомеров с калием можно записать одним уравнением:
2C7H7OH + 2K = 2C7H7OK + H2
В реакции фенола с калием масса фенола (4,18 – х) г, а объем выделившегося водорода
V(Н2) = z л.
2С6H5OH+2K=2C6H5OK+H2
Всего в реакциях выделилось 0,448 л газа: у + z = 0,448 л,
22,4х/(2*108) + 22,4*(4,18 – х)/(2*94) = 0,448.
Отсюда х = 3,24 г.
Масса фенола равна: 4,18 – 3,24 = 0,94 г.
Массовая доля фенола в смеси:
w(С6Н5ОН) = 0,94/4,18 = 0,225, или 22,5%.
Далее считаем сколько водорода выделилось при реакции с фенолом и по разности находим объем водорода выделяемый смесью бензилового спирта и крезола массой 3,24 г. Составляем еще одну систему уравнений.
_______________________________________________________________________________________________________________
Как видите, все задачи на фенолы сводятся к отличительным особенностям их химических свойств.
Задачи на спирты
Спирты в органической химии довольно разные и, соответственно, отличаются по химическим свойствам. Давайте рассмотрим основные примеры .
Задачи на спирты
Осуществить цепочку превращений
Осуществить цепочку превращений
Допустим, нам в задании С3 ЕГЭ по химии дана такая цепочка превращений:
Какой вообще алгоритм действий при решении таких задач?
Названия спиртов
У спиртов общая формула:
Однако,
Названия спиртов
очень отличаются, как и их свойства
Спирты и фенолы
Задачи на спирты и фенолы
Все задачи на тему спирты и фенолы сводятся к определению различий их химических свойств. Не смотря на то, что спирты и фенолы имеют одну функциональную группу -OH, различие в строении радикала R приводит к разным химическим реакциям.