Свойства алкенов
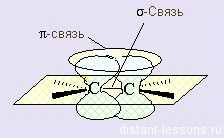
Когда мы говорили об алканах, упоминалась насыщенная связь. У алкенов эта связь ненасыщенная, двойная связь — этим определяются все свойства алкенов. Эта связь видоизмененных (= гибридизированных) орбиталей:
Sp² — гибридизация
Получается, что по двойной связи молекула имеет плоскость. Радикалы при двойной связи будут располагаться по обе стороны от этой плоскости.
Общая формула алкенов:
CnH2n
n = числу атомов углерода.
Номенклатура алкенов строится из двух частей.
Первая часть «говорит» о количестве атомов углерода, вторая — о связи -С=С-. У алкенов вторая часть всегда имеет окончание -ен.
По правилам номенклатуры ИЮПАК:
- в качестве основной цепи выбирается та, в которой находится двойная связь, не зависимо от ее размера,
- нумерация идет с того конца, к которому ближе двойная связь
- после окончания -ен ставится номер атома, после которого идет двойная связь.
Соответственно, существует 3 вида изомерии алкенов:
- Структурная
- Пространственная
- Межклассовая
Структурная изомерия алкенов: ну, во первых, можно по цепи двигать двойную связь — изомерия положения двойной связи:
во-вторых, изомерия положения радикалов:
Пространственная изомерия: это положение одинаковых радикалов при двойной связи либо по одну, либо по разные стороны от плоскости двойной связи: цис- \транс-изомерия:
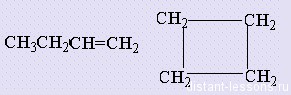
Межклассовая изомерия алкенов: по общей формуле — СnH2n алкены изомерны циклоалканам.
Химические свойства алкенов:
Двойная ненасыщенная связь обуславливает такие свойства алкенов, как реакции присоединения — π- связь разрывается и образуется одинарная — алкены превращаются в алканы.
- Реакции присоединения:
- СH2=CH-CH3 + H2 → CH3-CH2-CH3
- CH2=CH-CH3 + Br2 → CH2Br-CHBr-CH3 — качественная реакция на алкены — обесцвечивание бромной воды.
- Присоединение по правилу Марковникову:
водород присоединяется к наиболее гидрогенезированному (= к тому, у которого больше водородов) атому углерода при двойной связи:
СH2=CH-CH3 + HCl = CH3-CHCl-CH3
- Окисление алкенов:
- В нейтральной (или слабощелочной среде:
СH2=CH2 → CH2(OH) — CH2(OH) — схематичное уравнение
3СH2=CH2 + 2KMnO4 + 4H2O = 3C2H4(OH)2 + 2MnO2 + 2KOH — полное уравнение - В кислой среде — идет разрыв двойной связи:
R-СH=CH-R → 2R-COOH — схематичное уравнение - полное сгорание: С2H4 + 3O2 = 2CO2 + 2H2O
- В нейтральной (или слабощелочной среде:
- Реакция полимеризации:
n СH2=CH2 → n(-CH2-CH2-)
Получение алкенов:
Алкены получают двумя способами:
- Гидрирование алкинов: C2H2 + H2 = C2H4
- из производных алканов: дегидрирование, дегалогенирование, дегидрогалогенирование и т.д.
- в ЕГЭ это вопрос А13 и А14 — Строение и свойства углеводородов
- в ГИА (ОГЭ) это B2 — Первоначальные сведения об органических веществах: предельных и непредельных углеводородах
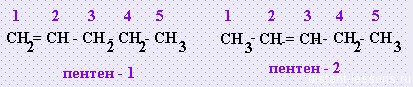
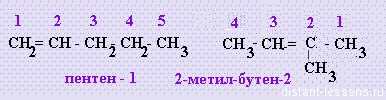


Здравствуйте!Небольшая опечатка в таблице получения алкенов — Алканы-де-…де-…
спасибо! исправим
Здравствуйте, можете помочь со следующими заданиями:
1) Классификация этиленовых углеводородов( не представляю, что там может быть. Может какие из них являются газами, жидкостями и твердыми вещесвами)
2) Уравнение реакции гидробромирования пентена-2( вопрос в том, куда будет присоединяться водород, а куда бром, и почему. Я знаю, что есть правило Морковникова, но здесь оба атома углерода одинаково гидрогенизированы)
3) Написать формулЫ и названия дигалогенпроизводных из которых при взаимодействии с цинком получается 4-этил-2-метилпентен-1( эти формулы будут отличаться только галогенами, или же может быть какое-то отличие в строении? И все-ли галогены могут тут присутствовать?)
Доброго времени суток!
1) по классификации — можно ответить про изомеры -на сайте есть по этому вопросу информация
2) Пентен-2: СH3-CH=CH-CH2-CH3 — водород может пойти как ко второму атому С, так и к 3. Суть в том, что на практике всегда образуется смесь изомеров.
3) 4-этил-2-метилпентен-1: СH2=С(CH3)-СH2-СH(C2H5)-СH3 будет образовываться из СH2Cl-CCl(CH3)-СH2-СH(C2H5)-СH3 , можно дибромпроизводное взять, разницы нет.
Получается, что в 3) можно брать любые галогены?
да, любые
СH3-CH2-CH=CH-CH3+HOH —>CH3-CH2-CH(OH)-CH2-CH3
почему так? с учетом индуктивного эффекта. Метильная группа сильнее оттягивает электронную плотность пи-связи, чем этил. Поэтому у третьего углерода дельта плюс, а у второго — дельта минус. В молекуле воды у водорода — дельта плюс, а у гидроксильной группы дельта минус. Поэтому водород воды идет ко второму углероду, а гидроксильная группа — к третьему/ аналогично гидрогалогенирование идет
Вы правильно написали. Должно быть СH3-CH2-CH=CH-CH3+HOH —>CH3-CH2-CH2-CH(OH)-CH3