Задачи на массовую долю вещества в растворе
Задачи на массовую долю вещества в растворе
Есть очень простая формула массовой доли — масса части разделить на массу целого, но в задачах на нахождение массовой доли в растворах есть несколько небольших, но очень существенных нюансов.
Давайте рассмотрим несколько примеров задач на эту тему.
1. Выделение газа из среды реакции:
В задачу закралась опечатка — дан нитрат калия, а получают карбонат натрия… давайте сделаем расчет на натрий.
Запишем реакцию: Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑ + H2O
В результате реакции выделяется углекислый газ — CO2. Обозначим массу полученной соли m,
n(NaNO3)= m\Mr = m\ 85 моль.
Тогда, по уравнению реакции количество азотной кислоты будет равно количеству соли:
n(HNO3) = n (NaNO3)= m \85 моль.
m(HNO3)= Mr•n = 63 •m \85 г
Это количество вещества, вступившего в реакцию, нам дано, что это количество соответствует 6.3 %, значит, масса 100% — масса раствора азотной кислоты равна 63 •m •100\(6.3 •85) г
Формула массовой доли вещества в растворе:
m(вещества)=m(NaNO3)=63 •m \85 гА масса всего раствора будет слагаться из масс реагентов и надо вычесть массу выделившегося газа:
m( раствора HNO3) + m(Na2CO3)- m(CO2)
m(раствора)= 63 •m •100\(6.3 •85) + 106• m\ 2•85 — 44•m\ 2•85 = 1031•m\85 г
w=m(HNO3) \ m(раствора) =63 •m \1031• m = 0,0611 или 6.11%
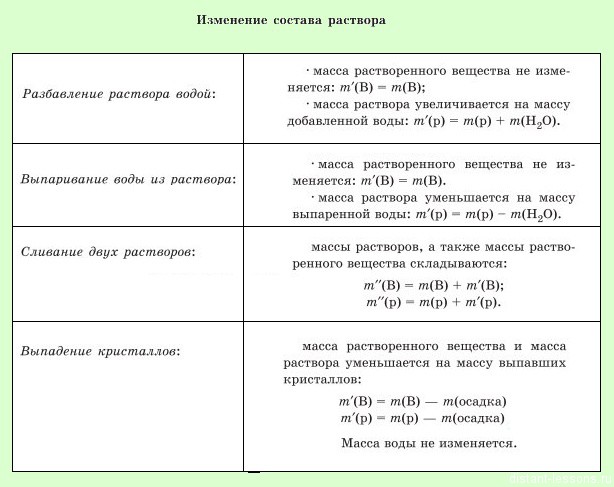
Важно понимать, что происходит при протекании заданной реакции — если выделяется газ, то он уходит из среды раствора, значит, при вычислении массовой доли надо вычесть массу газа из массы раствора.
2. Выпадение осадка:
Реакция: NaCl + AgNO3 = AgCl↓ + NaNO3
В ходе реакции выпадает осадок, значит, при расчете массовой доли, надо будет вычесть массу осадка из массы раствора.
m(NaCl)= m(раствора) • w = 117 • 0.05 = 5,85 г
n(NaCl)= m\Mr=5,85\58,5=0.1 моль
m(AgNO3)=m(раствора) • w=127.5 • 0.02 = 2,55 г
n(AgNO3)= m\Mr=2,55\170 = 0,015 моль
Т.к. количество молей двух реагентов не одинаковое, то надо решить, какое вещество дано в недостатке и по этому количеству молей рассчитать количество полученной соли.
NaCl + AgNO3 = AgCl↓ + NaNO3
0.1 моль 0.015 моль -> 0.015 моль
Очевидно, что хлорид натрия у нас в избытке, значит, считаем по нитрату серебра — n(AgCl)=n(AgNO3 )=0.015 моль.
m(AgCl)=n•Mr=0.015•143,5=2,1525 г
Этот осадок уйдет из раствора, поэтому при вычислении массовой доли это число надо вычесть из массы раствора:
m(раствора) = m(раствора NaCl) + m(раствора AgNO3) — m(AgCl) = 117+127.5-2,1525=242,3475 г
Находим массовую долю вещества в растворе:
w=m(NaNO3) \ m(раствора)=1.275\242,3475 = 0,00526 или 0.526%










Помогите, пожалуйста, с задачей. Решала через X, но не получилось. Вроде, всё по логике делала…..К какой массе 18 %-го раствора сахара надо добавить 200 г 16 %-го раствора, чтобы получить 10 %-й его раствор?
массу раствора обозначаем за х
тогда 0.1 = (0.18х +200*0.16)\(х+200)
х=150
Спасибо Вам. Я решала точно так же и уравнение тоже такое, Х получается здесь отрицательным. Что-то не так?
Ну тут что-то с условием не корректно, потому что если вы добавляете к одному раствору другой примерно той же концентрации, то массовая доля не может уменьшится почти вдвое…. она будет либо примерно такая же, либо немного больше или меньше, поэтому получается отрицательный ответ.
Я тоже засомневалась в корректности условия, задание из Интернета. Логика решения, вроде, правильная. Но не очень уверена в себе.Спасибо большое.
Прорешайте побольше таких задач, но лучше не из инета брать, а из задачников или демо-версий ЕГЭ и тогда будет больше уверенность 🙂
Помогите решить задачи
⦁ Определите массу осадка, образовавшегося в результате реакции между 200 г 7%-ного раствора карбоната натрия и избытком раствора хлорида кальция
⦁ К раствору бромида бария прилили 180 г раствора сульфата калия и получили осадок массой 10,54 г. Какова массовая доля (%) сульфата калия в растворе
⦁ В результате реакции 60%-ного раствора азотной кислоты с серебром выделилось 4,48 мл оксида азота (IV). Вычислите массу израсходованного раствора азотной кислоты
1) Na2CO3 + CaCl2 = CaCO3 + 2NaCl
n(Na2CO3) = m(раствора)*0.07\M(Na2CO3)
n(CaCO3)=n(Na2CO3)
m(CaCO3)=n*M(CaCO3)
2) BaBr2 + K2SO4 = BaSO4 + 2KBr
n(BaSO4) = 10.54 г\ M(BaSO4)
n(BaBr2) = n(BaSO4)
m(BaBr2) = n*M
w(BaBr2) =m(BaBr2)\180 г
3)
Ag + 2HNO3 = AgNO3 + NO2 + H2O
n(NO2) = V\22.4 л\моль
n(HNO3)=n(NO2)
m(HNO3)=n*M
m( раствора HNO3) = m(HNO3)\0.6
Помогите, пожалуйста,с задачей: Сколько оксида хрома (III), содержащего 10% примесей, потребуется для получения 52 г хрома методом алюминотермии.
Cr2O3 + 2Al = Al2O3 + 2Cr
n(Cr) = m\Ar(Cr)
n(Cr2O3) = 1\2n(Cr)
m( чистого Cr2O3)=n*M(Cr2O3)
m( с примесями) = m( чистого Cr2O3) \ 0.9
Спасибо!
Помогите решить задачу, в образце технической криссталической соды массовая доля составляет 90%.,рассчитайте какова масса такой соды необходима для приготовления раствора объёмом 10дм3 с эквивалентно концентрацией карбонат натрия. 0,02 NA2CO3*10H2O
кол-во моль n=C*V
m=n*M(Na2CO3*10H2O)
массовая доля чего? Если чистого вещества 90%, то m (технической соды) = m\0.9
если примесей 90%, то m (технической соды) = m\0.1
Здравствуйте,помогите пожалуйста решить задачу,желательно все действия производить в одной целиковой формуле(не по действиям)
Рассчитайте массу (г) кристаллогидрата Li2SO4 . H2O, взятого для
приготовления 200 г 0,57 М раствора с плотностью 1,05 г/мл.
См = n (кол-во моль)\ V
V=m\p
Получаем, что m= M(Li2SO4*H2O)*Cм*m\p
Здравствуйте, помогите пожалуйста с задачей 7 класса Дано:
м(раствора)=300г
м(CuSo4)=0,2
W(H2O)-?
Посчитайте м(H2O)необходимую для 300г с массовой частью CuSo4 (II) 0,2
просто подставьте в формулу массовой доли:
w=m( вещества ) \ (m( вещества) + m(H2O)
m( вещества) = m (раствора)*w = 300*0.2
значит, масса воды = m (раствора)-m( вещества)
Здравствуйте, помогите, пожалуйста, решить задачу.
При сплавлении с гидроксидом натрия натриевой соли предельной одноосновной карбоновой кислоты получен газ. Установите его формулу, если массовая доля натрия в использованной соли равна 20,91%.
Добрый день!
R-COONa + NaOH = Na2CO3 + RH
M(RCOONa) = x+12+32+23 = x+67 г\моль
составляем пропорцию:
Ar(Na)= 23 г\моль — 20.91%
x+67 -100%
23*100 = 20.91*(x+67)
x=43 г\моль
т.к. кислота предельная, то R=CnH2n+1
т.е. 12*n+2n+1 = 43
n=3
газ — пропан
Спасибо большое!
Здравствуйте, помогите пожалуйста решить задачу. Рассчитайте, какова массовая доля (%) каждой из кислот в растворе, если для нейтрализации 20г раствора, содержащего муравьиную и уксусную кислоты, понадобилось 20г раствора NaOH с массовой долей 20%. При взаимодействии такой же массы раствора кислот с аммиачным раствором оксида серебра получено 10,8г серебра.
C аммиачным раствором оксида серебра будет взаимодействовать только муравьиная кислота, т.к. у нее есть альдегидная группа.
HCOOH + Ag2O → 2 Ag + CO2 + H2O
n(Ag) = m\Ar = 0,1 моль
по уравнению реакции n(HCOOH) = 1\2n(Ag) = 0.5 моль
C NaOH реагируют обе кислоты.
HCOOH + NaOH = H2O + HCOONa
СH3CCOH+ NaOH = H2O + CH3COONa
c 0.5 моль муравьиной кислоты прореагирует 0.5 моль NaOH
всего нам дано n(NaOH) = m*0.2 \ M(NaOH) = 0.1 моль
Значит, на реакцию с уксусной кислотой останется тоже 0.5 моль
Следовательно, n(CH3COOH) = 0.5 моль
Дальше находите массу каждой кислоты: m=n*M
а затем — массовую долю: w = 100%* m(вещества) \ m ( раствора)