Инертные газы
Посмотрим на периодическую систему химических элементов. Как вам известно, элементы, находящиеся в одной группе и одной подгруппе обладают схожими свойствами, например:
IА – группа щелочные металлы
VIA – группа халькогены
VIIA – группа галогены
В этой статье мы уделим внимание VIIIA-группе.
автор статьи — Саид Лутфуллин
Это элементы: гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) (это основные), а так же радиоактивный радон (Rn).
И формально сюда же можно отнести искусственно полученный унуноктий (Uuo).
У этой группы элементов тоже есть свое название – аэрогены, но чаще их называют благородные, или инертные газы.
Инертные газы
Эти газы объединяет низкая реакционная активность. Под словом инертность как раз и понимается малоактивность. Поэтому об их существовании долгое время даже не догадывались. Определить их с помощью реакций нельзя. Обнаружили их в воздухе (отсюда и название аэрогены), удалив из него кислород и прочие «побочные газы», чтобы получить азот, и экспериментально установили, что полученный таким образом азот имеет примеси. Примесями этими и оказались инертные газы.
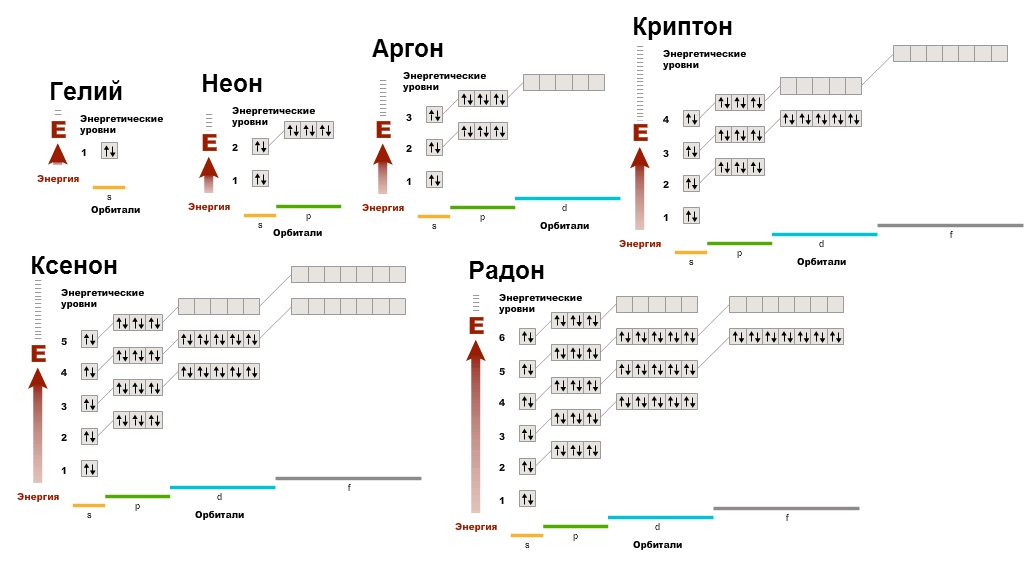
Чтобы понять, с чем связана низкая реакционная активность этих газов нужно построить их электронные диаграммы:
Мы можем видеть, что нет неспаренных электронов, орбитали заполнены. Это очень выгодное состояние электронной оболочки. Поэтому и все остальные элементы, образуя соединения, стремятся приобрести электронную конфигурацию благородных газов (вспомните правило октета), потому что она энергетически выгодная, а атомы, как и люди, выгоду любят.
Из-за малоактивности атомы благородных газов даже не соединяются в двухатомные молекулы (как это делают остальные газы: O2, Cl2, N2 и т.д.).
Благородные газы существуют в виде одноатомных молекул.
Говорить, что благородные газы абсолютно инертны нельзя. У некоторых аэрогенов есть свободные орбитали в пределах одного энергетического уровня, а это значит, что возможен процесс возбуждения электронов. В настоящее время в чрезвычайно экстремальных условиях получены некоторые соединения этих «ленивых» с точки зрения химической активности элементов. Но в школьной программе, а тем более в ЕГЭ, это не рассматривается.
Физические свойства
- гелий и неон легче воздуха, остальные благородные газы, которые находятся ниже – тяжелее, что обусловлено возрастанием атомной массы.
- из-за химической инертности, вкусовые и обонятельные рецепторы не могут обнаружить присутствие благородных газов в воздухе, поэтому они не имеют ни вкуса, ни запаха.
Практическая значимость благородных газов.
Гелий – всем хорошо известный газ, для заполнения воздушных шариков, который делает голос смешным. Гелием заполняют дирижабли (этот газ, в отличие от водорода, не взрывоопасен).
Благородные газы используют для создания инертной (химически не активной) атмосферы. Некоторые аэрогены входят в состав дыхательных смесей, разбавляя собой кислород (кислород – сильный окислитель и дышать им в чистом виде нельзя).
При пропускании через благородные газы разряда тока, они имеют свойство ярко светиться. Что обеспечивает аэрогенам применение для осветительной аппаратуры. Выглядит довольно зрелищно.