«Говорящие» кислотные остатки
«Говорящие» кислотные остатки
Когда я начинаю занятия по химии и рассказываю о Периодической системе элементов, то всегда говорю, что это как ключ от всех дверей. В ней можно найти ответ на практически любой вопрос по химии.
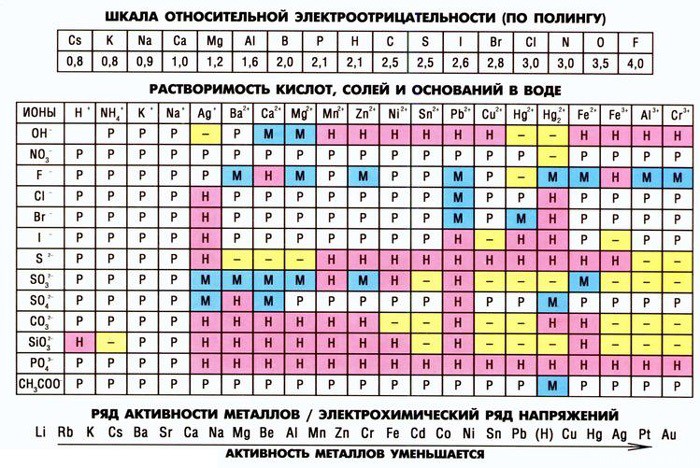
Таблица растворимости тоже в этом плане очень информативна. Здесь можно найти не только соли и узнать растворимы они или нет. Здесь есть еще один маленький секрет, который может оказаться очень полезным…
Давайте сегодня подробно рассмотрим левый столбец — столбик Анионов, или Кислотных остатков.
Во-первых, я считаю абсолютно необходимым знать названия и заряды кислотных остатков. В принципе, их можно легко вывести, но на экзамене у вас просто не хватит на это времени. Спорить с этим бесполезно. Это факт.
Поэтому, выучиваем:
OH(-) — гидроксид;
NO3(-) — нитрат;
F(-) — фторид;
Cl(-) -хлорид;
Br(-) — бромид;
J(-) — йодид;
S(-2) — сульфид;
SO3(-2) — сульфит;
SO4(-2) — сульфат;
CO3(-2) — карбонат;
SiO3(-2) — силикат;
PO4(-3) — фосфат;
CH3COO(-) — ацетат.
Во-вторых, обратите внимание, что все названия кислотных остатков имеют различие в окончаниях: —ид, -ит и -ат.
Окончания эти говорят о многом:
- -ид (кроме -OH): фторид F(-), хлорид Cl(-), бромид Br(-), йодид J(-), cульфид (-2):
- кислотный остаток состоит из одного элемента;
- этот элемент находится в минимальной степени окисления ( = № группы-8);
Поэтому даже если какого-то кислотного остатка нет в табличке, но у него окончание -ид, мы можем легко написать его формулу.
Например, нитрид алюминия: нитрид, значит, состоит из одного элемента — N, степень окисления минимальная=-3, значит, формула будет AlN.
- —ит: cульфит SO3(-2):
- кислотный остаток состоит из элемента и кислорода;
- элемент находится в средней степени окисления (в данном примере у серы S степень окисления +4)
Например, кислотного остатка нитрита в нашей таблице нет, но окончание -ит, значит это азот и кислород NO, промежуточная степень окисления азота= +3, кислотный оксид будет N2O3, прибавим воду: N2O3 + H2O = 2HNO2, значит, кислотный остаток — NO2(-).
- -ат: сульфат SO4(-2), карбонат CO3(-2), силикат SiO3(-2), фосфат PO4(-3), ацетат CH3COO(-):
- кислотный остаток состоит из элемента и кислорода;
- этот элемент находится в максимальной степени окисления ( = № группы);
Например, кислотный остаток хлорат. Два элемента ClO. Максимальная степень окисления хлора Cl= +5. Кислотный оксид будет иметь вид Cl2O5. Кислота: Cl2O5 + H2O = 2HClO3. Кислотный остаток — ClO3(-).
Как видите, все можно вывести, но стоит ли тратить на это время? Но, бывает, что в заданиях попадаются кислотные остатки, которых нет в таблице растворимости или просто вы их не знаете. Что делать тогда? Выводить их формулу по указанной логике.
Кислотные остатки тоже оказались «говорящими»!




Исправьте фофат!
спасибо! сейчас исправим! 🙂
У вас ошибка. Хлораты анионы имеют формулу ClO3(-) и степень окисления хлора +5. . Кислотный остаток ClO4 имеет название перхлорат (что означает над хлоратом, сверх хлорат)
Большое спасибо, что обратили внимание! Исправили! Изначально планировалось написать про перхлорат, но так даже лучше