Спирты и фенолы
Задачи на спирты и фенолы
Все задачи на тему спирты и фенолы сводятся к определению различий их химических свойств. Не смотря на то, что спирты и фенолы имеют одну функциональную группу -OH, различие в строении радикала R приводит к разным химическим реакциям.
Задача:
При действии избытка натрия на раствор фенола в метаноле выделилось 1176 мл газа (н. у.).
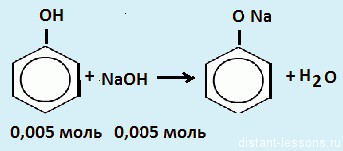
Для нейтрализации такого же количества раствора потребовалось 10 мл водного раствора NaОН с концентрацией 20 мг/мл.
Чему равна массовая доля фенола в исходном растворе?
Решение:
Для начала давайте распишем все химические процессы в задаче:
1. Во второй реакции проявляется то самое различие между спиртами и фенолами — из второй реакции, в которой метанол не взаимодействует с щелочью, мы можем найти количество моль фенола,
2. в условии сказано, что такое же количество прореагировало с Na в первой реакции — в этой реакции и спирт и фенол реагируют с Na одинаково.
3. Значит, мы можем найти то количество водорода (газ), которое соответствует фенолу,
4. найти остаток водорода и вычислить количество моль метанола.
В вопросе сказано найти массовую долю фенола, значит, используем стандартную формулу для массовой доли вещества в растворе
Давайте напишем подробное решение:
1. Дано 10 мл водного раствора NaОН с концентрацией 20 мг/мл. Значит, находим количество моль:
n (NaOH) = m\Mr=V*C(концентрация)\Mr = 10 (мл) * 0,020( г\мл) \40 (г\моль) \= 0,005 моль
Значит, по уравнению реакции, n(фенола) = 0,005 моль
2. Значит, количество фенола, вступившего в первую реакцию тоже 0,05 моль
3. Водорода по уравнению реакции получается в 2 раза меньше, чем фенола:
4. При действии избытка натрия на раствор фенола в метаноле выделилось 1176 мл газа (н. у.). Нам нужно найти количество моль водорода.
n(H2)=V\22,4 (л\моль) = 1.176 (л)\ 22.4 (л\моль) = 0.0525 моль
Значит, в реакции с метанолом выделилось 0.0525 — 0.0025 = 0,05 моль водорода
n (метанола) = 0.1 моль
Находим массовую долю:
m(фенола) = 0,05 (моль)*94 (г\моль) = 0,47 г
m(метанола) = 0,1 (моль) * 32 (г\моль) = 3,2 г
w(фенола) = m(фенола) \ (m(фенола) + m(метанола) )*100%= 0,47 (г)\ 3,67 (г)*100% = 12,8%
Обратите внимание, самая важная часть решения задачи состояла в определении различий реакций между спиртами и фенолами. Все остальное было — классические формулы для решения всех задач по химии…