Соединения ртути
Ртуть — элемент побочной подгруппы второй группы шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80. Обозначается символом Hg (лат. Hydrargyrum). Простое вещество ртуть — переходный металл, при комнатной температуре представляет собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты.
Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии
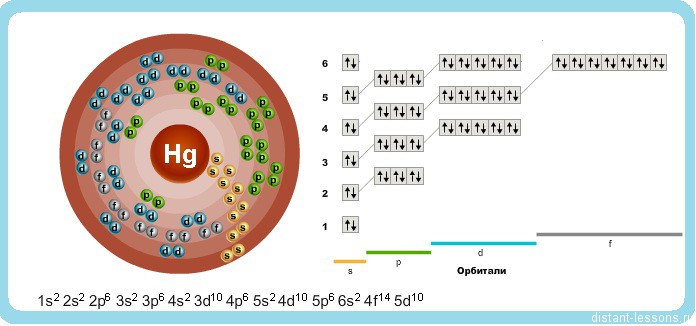
Исходя из электронного строения, можно сделать вывод, что для в соединениях ртуть будет проявлять степени окисления +2 и +1.
Физические свойства ртути:
- при комнатной температуре — сербристо-серая жидкость, легко переходящая в газообразное состояние;
- электро- и теплопроводна;
- очень высокая плотность вещества;
Как видите, все вышеперечисленные свойства — характеристики металлического вещества, хотя и в жидком состоянии.
Химические свойства ртути:
1) Реакция с кислородом (при нагревании >300 ° С): 2Hg + O2 = 2HgO (красного цвета);
2) реагирует с водородом, но только с атомарным ( так же при нагревании): Hg + 2H = HgH2 — гидрид ртути;
3) C неметаллами ( при нагревании): Hg + S = HgS
4) Взаимодействие с кислотами: с кислотами-не окислителями не взаимодействует

В ряду активности металлов ртуть стоит после водорода, поэтому в реакциях с кислотами-окислителями водород не выделяется:
Hg + 4HNO3 = Hg(NO3)2 + 2NO2 + 2H2O
Hg + 2H2SO4 = HgSO4 + SO2 + 2H2O
Как видно из реакции, чаще всего в соединениях ртуть проявляет степень окисления + 2, но +1 тоже встречается, причем в очень необычном виде:
|
Степень окисления |
Соединения ртути |
|
+1 |
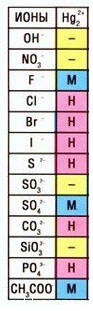
Оксид — не выделен; Гидроксид — не выделен Катион ртути — Hg22+ , соответственно, соль — нитрат ртути (I) — Hg2(NO3)2 Кстати, таких соединений ртути (I) немало — смотрите таблицу растворимости: |
|
+2 |
Соединения ртути (II) намного чаще встречаются в заданиях школьного курса химии: Оксид — HgO (относят к слабым основным или даже амфотерным оксидам);Гидроксид — не выделен Что касается соединений ртути (II), то не смотря на то, что простое вещество ртуть — металл, в веществах HgS (черные или красные кристаллы) и HgJ2 (желтые кристаллы) cвязь ковалентная. Связь ртуть-углерод в органических соединениях ртути самая прочная из всех известных металл-органических связей |
Соединения ртути чрезвычайно ядовиты, соответственно, как и большинство других ядов, их часто используют в медицине:
- хлорид ртути (I) (каломель) — слабительное;
- меркузал и промеран — сильные мочегонные;
- хлорид ртути (II), цианид ртути (II), амидохлорид ртути и жёлтый оксид ртути(II) — антисептики (в том числе в составе мазей).
- Амальгаму серебра применяют в стоматологии в качестве материала зубных пломб.




Ввиду чрезвычайной токсичности современная медицина как лекарства соединения ртути не использует вообще. Перечисленные тутные диуретики сняты в производства в конце 60х годов, ртутные антисептики также более не используются — тем более, что в современных условиях имеется море аналогичных по эффекту, но практически нетоксичных и поэтому безопасных синтетических веществ.