Свойства спиртов
Свойства спиртов
Все органические соединения, имеющие одну или несколько групп -OH, относят к спиртам:
R—OH
Классификация спиртов:
1) Спирты подразделяют на одно- и многоатомные — по количеству гидроксильных групп (-групп -OH);
2)Еще одна классификация — по атому С, к которому крепится группа -OH: первичные, вторичные и т.д.
Номенклатура
или как правильно все это назвать
Для одноатомных спиртов
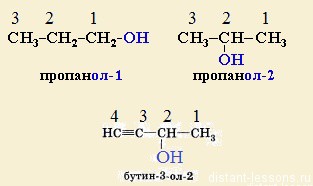
I Вариант номенклатуры: общее название: название R + “-ол” (метанол)
1. Углеродная цепь нумеруется с того края, к которому ближе -OH группа
2. Положение -OH группы указывается после окончания “- ол”
3. “Внутри”радикала правила номенклатуры те же, что и в углеводородах
II Вариант номенклатуры: название радикала + “-овый” + “спирт”
(метиловый спирт, бутиловый спирт, изобутиловый спирт)
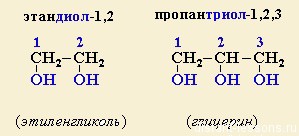
Для многоатомных спиртов:
положение -OH групп + “-ди” + ”три”… + “-ол”
Изомерия спиртов
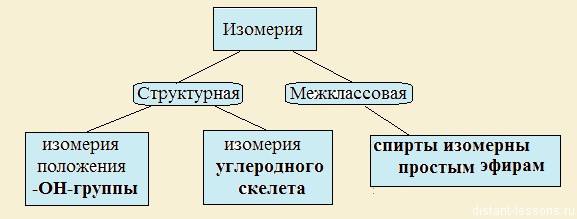
1. Структурная изомерия
-
Начиная с С3 — изомерия положения гидроксильной группы:
-
Начиная с С4 — углеродного скелета
2. Межклассовая изомерия — у спиртов и простых эфиров одна и та же общая формула:
Физические свойства спиртов:
Все спирты С1-С11- жидкости, т.к. для них возможно межмолекулярное взаимодействие — водородная связь:
- У них “алкогольный вкус” и они хорошо растворимы в воде
-
С С12 спирты становятся твердыми веществами
Соответственно, растворимость уменьшается
Химические свойства спиртов
Химические свойства определяются двумя частями молекул спиртов: радикала R и -OH-группы.
С R все просто: у него химические свойства соответствующего углеводорода.
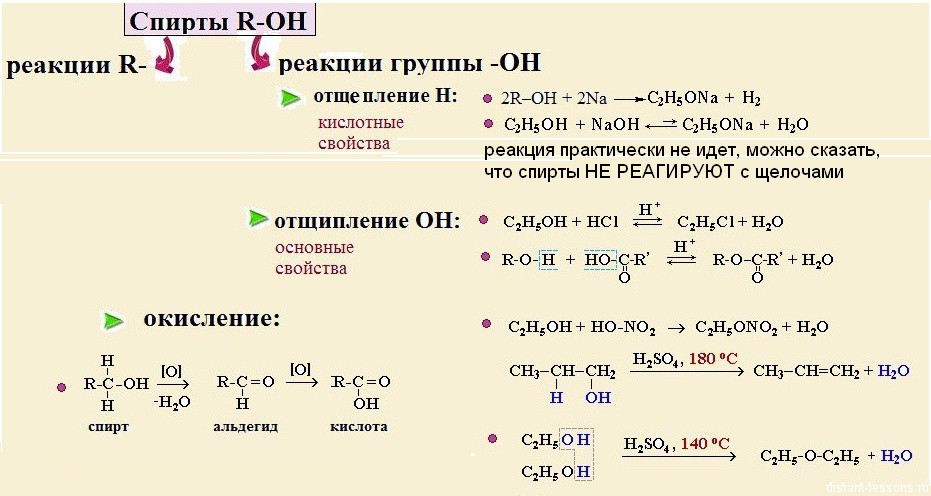
А с группой -OH картина следующая:
Схема отражает общие реакции и свойства спиртов.
Давайте рассмотрим их поподробнее:
Во-первых, реакционная способность у спиртов различная:
1. Кислотные свойства спиртов: кислотные свойства — это как раз способность отщеплять водород H.
Поэтому спирты взаимодействуют с металлами и щелочами:
- с металлами реакция идет бурно, т.к. выделяется газообразный водород;
- с щелочами — еле-еле, т.к. алкоголяты — соли спиртов довольно хорошо гидролизуются:
- многоатомные спирты реагируют точно так же:
Качественная реакция на многоатомные спирты:
- реакции образования эфиров — как простых, так и сложных, называются реакциями этерификации.
- реакции окисления обычно не имеют каких-либо «подводных камней», за исключением того, что в части С (ЕГЭ) их надо уравнивать методом полуреакций.
- «предельное окисление» спиртов — реакция горения:
2. Основные свойства спиртов (отщепление -OH-группы):
Здесь тоже разная реакционная способность:
третичные > вторичные > первичные > метанол
- дегидратация: внутримолекулярная (180 С, образование алкенов)
- дегидратация: межмолекулярная (140 С, образование простых эфиров)
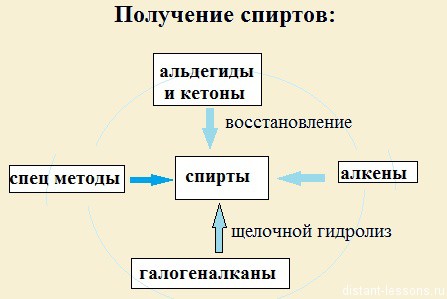
Получение спиртов
К специальным методам можно отнести:
- получение из глюкозы
- получение метанола из водорода и угарного газа
- в ЕГЭ это вопрос А14 — Свойства предельных одноатомных и многоатомных спиртов, фенола
- в ГИА (ОГЭ) это B2 — Первоначальные сведения об органических веществах: кислородсодержащих веществах: спиртах
[TESTME 47]



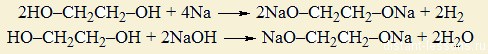
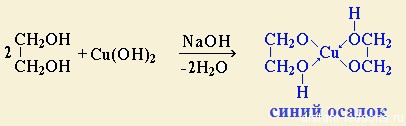
Лолита Витальевна, помогите пожалуйста разобраться! Как будет протекать внутримолекулярная дегидратация такого вот спирта:
Как применить правило Зайцева? По идее тут может образоваться как гексен-2, так и гексен-3.
http://www.xumuk.ru/rhfr/148931.gif
Да, тут возможен и гексен-2, и гексен-3 — по правилу Зайцева.
Обычно в реальных процессах так и происходит — образуется смесь изомеров.
Это вопрос из ЕГЭ? Обычно там стараются давать вопросы с однозначным ответом…
Нет, это вопрос не из ЕГЭ. Просто мне стало интересно, как будет применяться правило Зайцева, если выделить самый негидрогенизированный атом углерода нельзя.
Спасибо за ответ!